 Dr. Paul Kaye atualmente é professor titular da Universidade de York e pesquisador Sênior Welcome Trust. Tem sido mentor de diversos estudantes de pós-graduação e atua ativamente no desenvolvimento de novos recursos humanos para a ciência. Pesquisador de renome, entre suas linhas de pesquisa estuda, principalmente, a interação parasito-hospedeiro na leishmaniose. Dr. Kaye avalia esta interação no organismo ao invés de abordagem meramente celular. Além disso, já publicou inúmeros trabalhos de grande impacto sobre este tema, contribuindo de forma valiosa para a comunidade científica.
Dr. Paul Kaye atualmente é professor titular da Universidade de York e pesquisador Sênior Welcome Trust. Tem sido mentor de diversos estudantes de pós-graduação e atua ativamente no desenvolvimento de novos recursos humanos para a ciência. Pesquisador de renome, entre suas linhas de pesquisa estuda, principalmente, a interação parasito-hospedeiro na leishmaniose. Dr. Kaye avalia esta interação no organismo ao invés de abordagem meramente celular. Além disso, já publicou inúmeros trabalhos de grande impacto sobre este tema, contribuindo de forma valiosa para a comunidade científica.
Tag: Leishmania
The Journal of Immunology publica estudo sobre degranulação de neutrófilos para controle do L. amazonensis
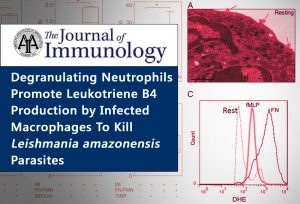 O artigo Degranulating Neutrophils Promote Leukotriene B4 Production by Infected Macrophages To Kill Leishmania amazonensis Parasites, publicado no periódico científico The Journal of Immunology, em 22 de janeiro, aborda um estudo realizado por pesquisadores da Fiocruz Bahia, acerca do efeito da degranulação de neutrófilos sobre macrófagos infectados com o parasita Leishmania amazonensis. O estudo demonstrou que neutrófilos ativados interagem com macrófagos infectados levando a um aumento do seu poder microbicida, principalmente pelo eicosanoide chamado leukotrieno B-4.
O artigo Degranulating Neutrophils Promote Leukotriene B4 Production by Infected Macrophages To Kill Leishmania amazonensis Parasites, publicado no periódico científico The Journal of Immunology, em 22 de janeiro, aborda um estudo realizado por pesquisadores da Fiocruz Bahia, acerca do efeito da degranulação de neutrófilos sobre macrófagos infectados com o parasita Leishmania amazonensis. O estudo demonstrou que neutrófilos ativados interagem com macrófagos infectados levando a um aumento do seu poder microbicida, principalmente pelo eicosanoide chamado leukotrieno B-4.
Os neutrófilos são células sanguíneas que fazem parte do sistema imunológico, eles são responsáveis pelas primeiras respostas contra os patógenos e são ativados durante a transmigração endotelial para o local da inflamação. Na presente pesquisa, os neutrófilos humanos foram ativados in vitro com proteínas de matriz extracelular imobilizadas, tais como a fibronectina (FN), colágeno, laminina e somente a ativação de neutrófilos por FN, induziu a libertação do conteúdo dos grânulos.
Os resultados mostram que o tratamento de neutrófilos humanos com FN in vitro induz a degranulação e produção de ROS (do inglês, espécies reativas de oxigênio), enquanto em repouso, eles permaneciam não ativados. Foi detectada uma maior produção de ROS em neutrófilos tratados com FN; além da liberação da enzima MMP-9 e aumento da atividade da elastase neutrofílicae (NE), em comparação com células em repouso ou outras proteínas.
A partir deste conjunto de resultados, os estudiosos puderam concluir que a fibronectina induziu uma ativação mais eficiente de neutrófilos, a presença de neutrófilos ativados com FN diminui a carga parasitária de macrófagos infectados por L. amazonensis. Além disso, resultados sugerem que a diminuição da infecção em macrófagos é independente do contato da célula e pode ser intermediada por mediadores solúveis. O leukotrieno B-4 tem um papel fundamental na ativação do macrófago induzindo a produção de TNf-alfa, essencial para a morte parasitária.
Participaram do estudo os pesquisadores da Fiocruz Bahia Natália Tavares, Lilian Afonso, Martha Suarez, Mariana Ampuero, Deboraci Brito Prates, Théo Araújo-Santos, Manoel Barral-Netto, Valéria Matos Borges e Cláudia Brodskyn.
Clique aqui para ter acesso ao trabalho.
Infectious Diseases publica artigo sobre bioassinaturas entre pacientes com leishmaniose tegumentar
 O estudo coordenado pela pesquisadora da Fiocruz Bahia Valéria Borges, sobre a associação do perfil de produção de eicosanoides em diferentes manifestações clínicas da leishmaniose tegumentar, foi publicado no The Journal of Infectious Diseases. No artigo Differential Expression of the Eicosanoid Pathway in Patients With Localized or Mucosal Cutaneous Leishmaniasis, os pesquisadores descrevem como identificaram uma bioassinatura inflamatória distinta in situ e sistêmica entre os pacientes com leishmaniose cutânea localizada (LCL) e a forma clínica mucocutânea (LCM).
O estudo coordenado pela pesquisadora da Fiocruz Bahia Valéria Borges, sobre a associação do perfil de produção de eicosanoides em diferentes manifestações clínicas da leishmaniose tegumentar, foi publicado no The Journal of Infectious Diseases. No artigo Differential Expression of the Eicosanoid Pathway in Patients With Localized or Mucosal Cutaneous Leishmaniasis, os pesquisadores descrevem como identificaram uma bioassinatura inflamatória distinta in situ e sistêmica entre os pacientes com leishmaniose cutânea localizada (LCL) e a forma clínica mucocutânea (LCM).
A leishmaniose tegumentar é uma doença transmitida por mosquito vetor, causada pelo parasita Leishmania, tendo como principal agente etiológico no Brasil a Leishmania braziliensis. Os eicosanoides participam da resposta imune como potentes mediadores da inflamação. A equipe de especialistas realizou um estudo exploratório transversal para avaliar se a via biossíntese dos eicosanoides no sítio da lesão cutânea e no plasma poderia estar associada a uma bioassinatura distinta entre as manifestações clínicas de pacientes com LCL e LMC.
Dessa forma, identificou-se que a expressão de enzimas e receptores e os níveis plasmáticos de prostaglandinas estão aumentados em LCL, enquanto os marcadores da via de lipoxigenases estão destacados em LCM. Os resultados indicaram que o balanço inflamatório entre leucotrienos e prostagladinas, principalmente a PGE2, poderia em parte contribuir para a imunopatogênese de LCL e LCM, servindo como alvos potenciais para futuras terapias direcionadas ao hospedeiro.
O estudo foi tema da tese de doutorado de Jaqueline França-Costa (Programa de Pós-gradução em Patologia Humana da Fiocruz Bahia/UFBA) e contou com o financiamento do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq). Dentre os autores do estudo, estão os pesquisadores da Fiocruz Bahia Bruno B. Andrade, Ricardo Khouri, Johan Van Weyenbergh, Hayna Malta-Santos, Claire da Silva Santos, Cláudia I. Brodyskn, Jackson M. Costa, Aldina Barral, Viviane Boaventura e Valeria M. Borges.
Clique aqui para acessar o artigo.
Combinação de medicamentos é aposta contra leishmanioses
Na busca por um tratamento para as leishmanioses que dispense o uso de injeções e tenha menos efeitos colaterais, pesquisadores do Instituto Oswaldo Cruz (IOC/Fiocruz) estudam o uso combinado de dois medicamentos que já estão disponíveis no mercado. Apesar de terem sido desenvolvidos para outros fins, o antidepressivo imipramina e o antifúngico miconazol têm potencial para agir contra os protozoários do gênero Leishmania, que causam a doença. Em um artigo publicado na revista Parasites & Vectors, os cientistas do Laboratório de Bioquímica de Tripanosomatídeos do IOC/Fiocruz apontam que esses fármacos de uso oral parecem agir através de mecanismos complementares. Os testes realizados em culturas de células – primeira etapa nas pesquisas de novos remédios – indicam que a combinação dos compostos permitiria utilizar doses reduzidas para combater os micro-organismos.
“Os produtos que já são licenciados passaram por testes de segurança que estão entre as etapas mais difíceis e caras do desenvolvimento de fármacos. Por isso, o reposicionamento de medicamentos é uma estratégia importante na busca por novas terapias, principalmente contra doenças negligenciadas como as leishmanioses”, explica Eduardo Caio Torres Santos, pesquisador do Laboratório de Bioquímica de Tripanosomatídeos do IOC/Fiocruz e coordenador do trabalho. “A imipramina e o miconazol são conhecidamente seguros. Ao associar as duas substâncias e reduzir as doses, podemos diminuir também os riscos de efeitos colaterais do tratamento”, acrescenta Valter Andrade Neto, pós-doutorando do mesmo Laboratório e primeiro autor do artigo.

Causadas por diferentes espécies de parasitos do gênero Leishmania, as leishmanioses podem se apresentar na forma cutânea, com feridas na pele; mucosa, com lesões na boca e no nariz; ou visceral, com danos em órgãos como fígado e baço. Em todos os casos, o tratamento da infecção costuma ser baseado nos antimoniais pentavalentes, uma classe de remédios utilizada desde a década de 1940, que pode causar diversos efeitos colaterais, incluindo danos ao coração, fígado, pâncreas e rins. Os remédios estão disponíveis apenas em formulações intravenosas e intramusculares, o que demanda a administração por um profissional de saúde. Além disso, nos casos em que os parasitos apresentam resistência aos medicamentos antimoniais, é necessário recorrer a fármacos ainda mais tóxicos, como a anfotericina B e a pentamidina.
Mecanismo de ação: achado inédito
Embora o potencial leishmanicida da imipramina tenha sido observado na década de 1980, seu mecanismo de ação contra os parasitos ainda não tinha sido descrito e a combinação com outras substâncias também nunca havia sido testada. Os experimentos feitos com a espécie Leishmania amazonensis – uma das causadoras da forma cutânea da infecção – apontam que o fármaco impede a síntese de uma molécula fundamental para a sobrevivência dos parasitos: o ergosterol, tipo de lipídeo que compõe a membrana dos micro-organismos, além de participar de vias de sinalização intracelular. De forma inédita, a pesquisa indica que a imipramina tem a capacidade de inibir uma enzima da L. amazonensischamada de C24-metiltransferase, que atua na fase final da síntese do ergosterol. “Este é um alvo interessante porque o ergosterol não é produzido em células de mamíferos. Logo, um fármaco que afeta a síntese dessa molécula não deve prejudicar o organismo dos pacientes”, comenta Eduardo Caio.
Utilizado para combater infecções causadas por fungos, o miconazol também bloqueia a síntese do ergosterol nos parasitos, porém usando um mecanismo de ação diferente: ele age sobre a enzima conhecida como C14-desmetilase. De acordo com Valter, o fato de os dois fármacos atuarem em pontos distintos da mesma via bioquímica é positivo para o efeito antiparasitário. Nos testes, a combinação dos fármacos apresentou efeito aditivo, ou seja, a ação de um somou-se à do outro. “Verificamos que não existe antagonismo entre imipramina e miconazol. Com o efeito aditivo, existe o potencial de usar quantidades menores de cada um dos fármacos e obter um resultado melhor”, destaca o pós-doutorando.
Realizados com a forma amastigota do parasito L. amazonensis – a mesma etapa do desenvolvimento do parasito que é encontrada nos pacientes –, os experimentos mostraram que as doses isoladas de imipramina e miconazol necessárias para matar cerca de 50% dos parasitos têm a eficácia muito aumentada quando usadas em conjunto, chegando a eliminar 90% dos micro-organismos. Em comparação, para alcançar o mesmo resultado utilizando somente miconazol, seria necessário dobrar a dose. Os testes confirmaram ainda que as duas substâncias – tanto separadas, como combinadas – não apresentam efeitos tóxicos para os macrófagos, células de defesa dos mamíferos que são infectadas pelos parasitos.
Próximas etapas
Ressaltando que o estudo ainda está na fase inicial, os pesquisadores consideram que os resultados indicam que a imipramina pode ser útil para o tratamento das leishmanioses, principalmente através da combinação com outros medicamentos. Segundo eles, além de agir diretamente sobre as leishmânias, o fármaco possui a capacidade de inibir a chegada de colesterol até esses micro-organismos, o que pode contribuir para a eficácia da terapia – um aspecto que pretendem investigar nas próximas etapas do trabalho. “Assim como o ergosterol produzido pelos parasitos, o colesterol produzido pelas células dos mamíferos é uma molécula de lipídeo da classe dos esteróis. Em pesquisas anteriores, observamos que as leishmânias passam a captar mais colesterol quando a síntese do ergosterol é bloqueada por fármacos. Imaginando que esse pode ser um mecanismo de escape desenvolvido pelos parasitos, consideramos que a imipramina pode assumir um efeito ainda mais importante”, explica Valter.
Para Eduardo Caio, é possível que o antidepressivo se torne um coadjuvante na terapia das leishmanioses, potencializando o efeito de fármacos do grupo químico do miconazol – conhecidos como azóis. Segundo o pesquisador, as substâncias desse grupo são muito potentes contra os parasitos do gênero Leishmania nos testes em laboratório, mas alguns ensaios clínicos mostraram eficácia reduzida nos pacientes. “Os azóis são utilizados há muitos anos para o tratamento de infecções causadas por fungos. Se a associação com a imipramina conseguir resgatar esses medicamentos como opções terapêuticas para as leishmanioses, teremos um grande benefício”, afirma.
Leia mais na Agência Fiocruz de Notícias sobre as formas de transmissão, prevenção e tratamento das leishmanioses.
Trabalho sobre Leishmania é publicado na revista PlosOne
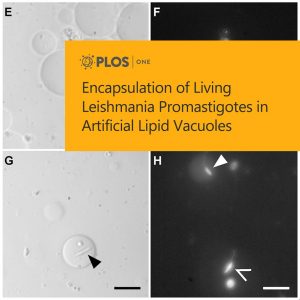
O trabalho “Encapsulation of Living Leishmania Promastigotes in Artificial Lipid Vacuoles” publicado na revista PlosOne, mostra pela primeira vez a encapsulação de promastigotas vivas de Leishmania em vesículas artificiais. Foi demonstrado que os parasitas podem sobreviver por dias, sendo possível ajustar a composição da vesícula, pH e temperatura. O Estudo, desenvolvido em um parceria entre o Laboratório de Patologia e Biointervenção (Fiocruz Bahia) e o Centre Interdisciplinaire de Nanoscience de Marseille (CINaM-Aix Marseille Université) abre perspectivas para o desenvolvimento de um modelo de vacúolo ex vivo para o estudo da amastigogênese e compreensão da influência do parasita no desenvolvimento do vacúolo parasitóforo.
Clique aqui para acessar a matéria.



